近日,上海科技大学生命科学与技术学院罗振革课题组于《分子治疗》(Molecular Therapy)在线发表题为“SEC62-mediated ER-Phagy activation alleviates Alzheimer's disease pathology and restores cognitive function in 5×FAD mice”的研究论文,深入揭示了内质网自噬受体SEC62在阿尔茨海默病(AD)病理进程中的关键调控作用,证实特异性激活SEC62介导的内质网自噬,能够显著缓解内质网应激、减少阿尔茨海默病密切相关的Aβ斑块沉积、抑制神经炎症,有效改善AD模型小鼠的认知损伤,为解析AD发病机制、发掘全新治疗靶点奠定了重要实验基础。
在全球老龄化背景下,阿尔茨海默病已成为最常见的神经退行性疾病之一。然而,其发病机制尚未完全阐明,临床上至今缺乏能有效延缓或逆转疾病进展的治疗策略。该病隐匿性极强,大多数药物无法顺利穿透进入脑部起效,也极大增加了特效药物研发与临床治疗的难度。内质网自噬(ER-phagy)作为一类选择性自噬途径,可特异性清除受损内质网,是维持内质网质量控制与稳态平衡的关键机制。前期研究发现,在阿尔茨海默病病理环境中,神经元内质网损伤显著,功能稳态被严重打破,但内质网自噬在阿尔茨海默病病理进程中的具体作用及调控机制仍有待进一步探究。
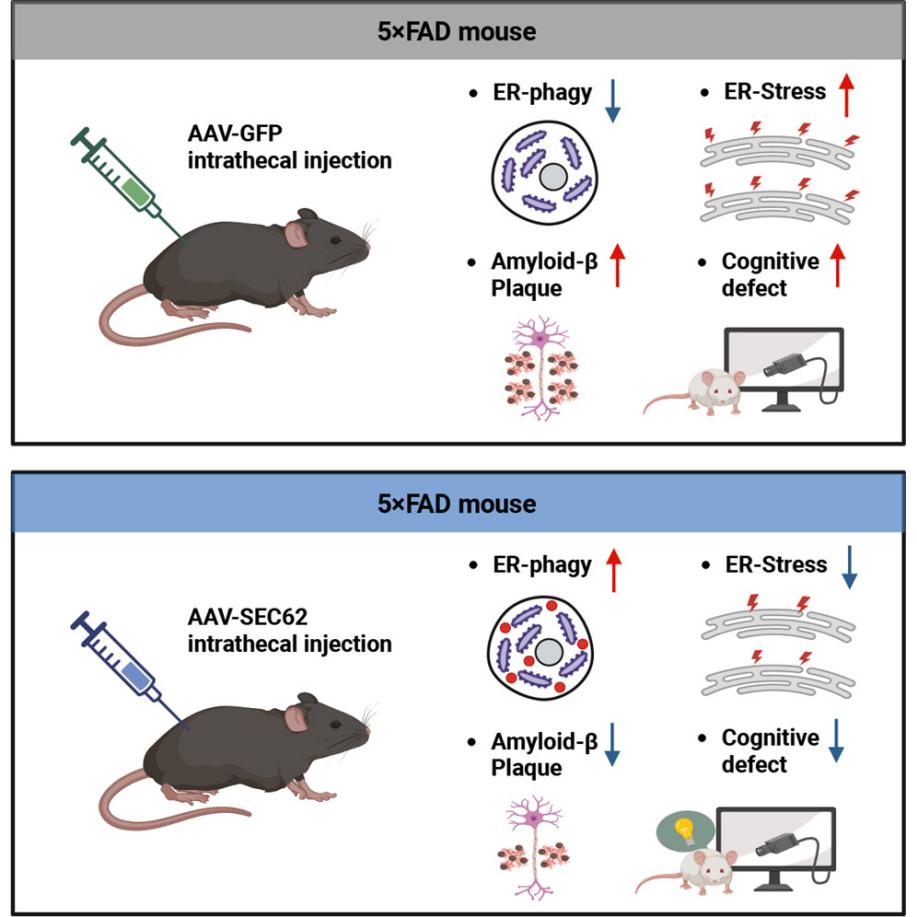
图注:SEC62通过激活内质网自噬改善5×FAD小鼠AD病理
为破解这一难题,研究团队依托多研究体系,对AD患者来源的iPSC分化神经元、临床患者测序数据及5×FAD转基因小鼠模型进行系统分析,明确证实AD病理环境下,神经元存在明显的内质网稳态失衡,具体表现为持续性内质网应激及细胞器结构损伤;利用内质网自噬特异性探针检测发现,AD神经元的内质网自噬功能存在缺陷。在此基础上,研究团队通过AAV鞘内递送技术,在AD模型小鼠脑内特异性过表达内质网自噬受体SEC62。结果证实,SEC62可有效恢复神经元的内质网自噬功能、缓解过度内质网应激,进而显著减少海马、皮层等重要脑区的Aβ斑块累积,同时抑制星形胶质细胞异常活化及脑内慢性神经炎症。行为学检测进一步表明,SEC62干预可有效改善AD小鼠的学习与记忆功能。
该研究系统阐明了内质网自噬受体SEC62在阿尔茨海默病病理进程中的关键调控作用,为挖掘全新AD干预靶点、研发创新治疗策略提供了重要的理论支撑与实验依据。
上海科技大学生命科学与技术学院罗振革课题组博士研究生黄晶为论文的第一作者,罗振革教授为论文通讯作者,上海科技大学为第一完成单位。
论文链接:https://www.sciencedirect.com/science/article/pii/S1525001626003023


 沪公网安备 31011502006855号
沪公网安备 31011502006855号