近日,上海科技大学信息科学与技术学院蔡夕然课题组与复旦大学智慧医疗超声实验室、联影医疗合作,在《IEEE超声学、铁电体技术与频率控制汇刊》(IEEE Transactions on Ultrasonics, Ferroelectrics, and Frequency Control)期刊在线发表了题为“Single Probe Enabled Refraction-Corrected Transcranial Passive Acoustic Mapping Through Macaque Calvaria”的研究成果,提出了一种基于单一超声探头阵列、无需CT支持的经颅折射校正被动声学成像(Transcranial Passive Acoustic Mapping, TPAM)新方法,可高效准确定位微泡(Microbubble, MB)空化声源,具备低成本、高准确性等特点,为脑部超声空化治疗的实时监测提供了全新的解决方案。
结合微泡空化的聚焦超声(Focused ultrasound, FUS)治疗技术,在血脑屏障开启、神经调节、神经再生以及脑部靶向药物递送等领域有着广泛应用前景。为了确保治疗的安全性和有效性,需要对微泡的空化行为进行实时监测,以防止其对周围神经组织和血管造成不可逆的损伤。被动声学成像(PAM)作为一种无创、高灵敏度的成像手段,可实时捕捉微泡空化所产生的声学信号,并重建其空间分布图像,已成为FUS治疗中监测空化活动的关键技术。然而,在穿越复杂的颅骨结构时,颅骨异质的声速分布会引起显著的声波折射和相位畸变,降低空化源定位的精度、影响超声聚焦定位与治疗剂量控制,可能削弱治疗效果、增加并发症发生风险。目前校正颅骨畸变误差的传统方法通常依赖额外的CT扫描来构建颅骨声速分布图,不仅增加了成像系统的硬件复杂度和成本,还面临CT与超声图像配准精度低、CT声速估算依赖经验关系等问题。
为克服上述挑战,研究团队提出了一种用于TPAM的全超声解决方案(图1)。方案通过纯超声手段构建颅脑声速分布并结合异质角谱算法,成功实现了无CT条件下的高精度声源定位。恒河猴颅骨实验证实方案显著降低了声源定位误差,提升了成像清晰度与主瓣能量集中度,在经颅声空化成像中的实用性与准确性得到验证(图2)。本方法可用于小动物及非人灵长类脑部超声成像,具有一定可扩展性和临床转化潜力。它为基于声空化效应的经颅血脑屏障开放监控和神经调控等研究方向提供了一种高效、无创、准确的空化活动可视化成像方案。未来有望扩展至经人颅骨的空化成像研究中,进一步推动FUS在脑疾病治疗中的临床转化。
上海科技大学是第一完成单位,上海科技大学硕士毕业生、现罗切斯特大学博士生金高飞和上海科技大学信息学院博士生曾一为共同第一作者,该工作由复旦大学他得安教授指导完成,蔡夕然教授和他得安教授为共同通讯作者。
文章链接:https://ieeexplore.ieee.org/document/11007027
DOI:10.1109/TUFFC.2025.3570971
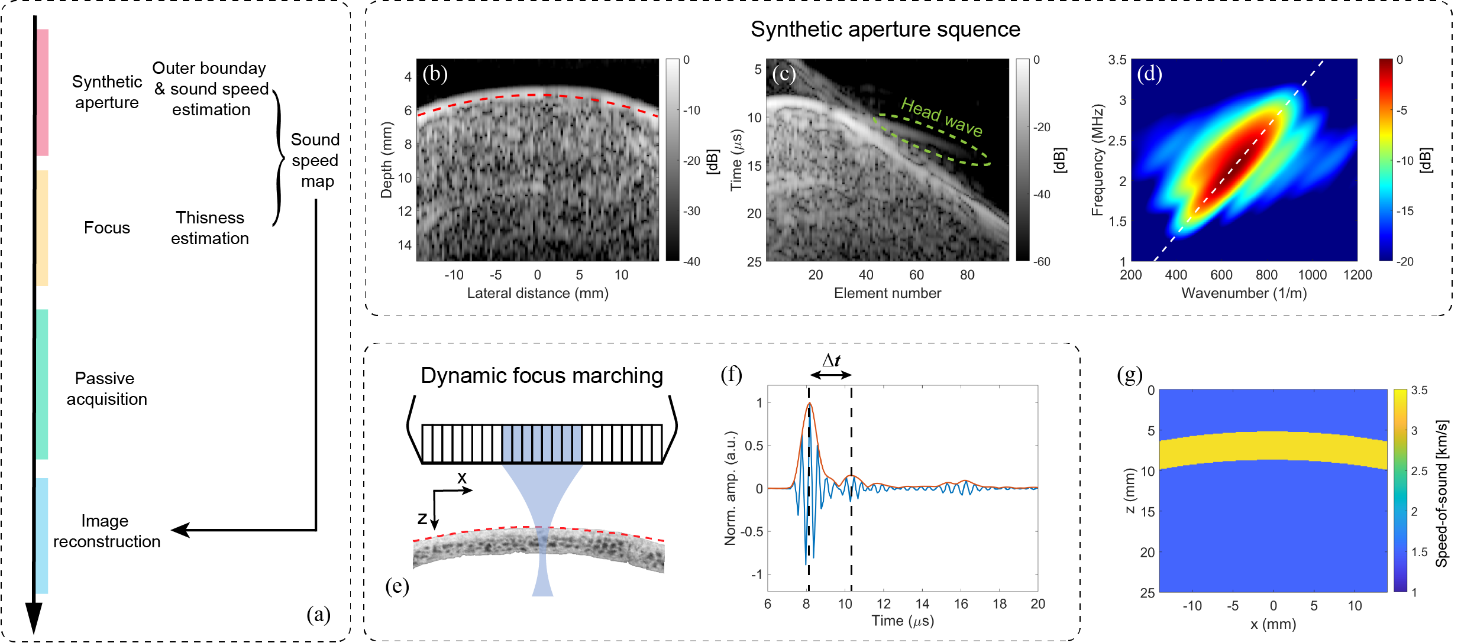
图1.基于单个超声探头的经颅折射校正被动声学成像重建方法。(a)数据采集与重建整体流程;(b)通过回波包络峰值提取头骨外边界(红色虚线);(c)第一阵元激发后的接收信号中包含首波信息;(d)对应的频率-波数(f-k)图,白色虚线拟合得到的斜率可转换为颅骨等效声速;(e)聚焦序列中,动态聚焦波束沿外边界轨迹移动;(f)在典型扫描线上检测颅骨内外表面的两个回波峰,用于厚度估算;(g)最终利用颅骨边界、声速和厚度重建声速图。

图2.水听器和微泡空化实验的被动声成像结果。


 沪公网安备 31011502006855号
沪公网安备 31011502006855号