近日,上海科技大学物质科学与技术学院高得伟课题组实现了链状、非连续1,3-立体中心的1,2-双硼酸酯的不对称合成。该工作解决了亲核试剂远离手性环境时构建非连续手性中心的难题,发展了偕二硼酸酯新的不对称催化反应模式,避免了两种经典阴离子中间体所导致的副产物生成。相关成果发表于国际化学领域代表期刊《德国应用化学》(Angewandte Chemie International Edition)。
药物与生物活性分子中普遍存在链状、非连续的1,3-立体中心,例如降血脂药物Rosuvastatin及降血压药物Aliskiren均含有该类手性骨架,但是围绕该类立体中心的直接构建一直进展缓慢(图1a)。近年来,不对称催化特别是利用协同催化策略在构建1,2-连续手性中心方面取得了长足进展。该反应往往利用有机小分子催化剂或Lewis酸催化剂控制亲核试剂的进攻方向,同时利用过渡金属和手性配体调控亲电试剂的立体选择性,高效构建四个立体异构体。但如果亲核试剂没有与有机小分子催化剂或者Lewis酸作用的位点时,通过单一催化剂调控立体选择性特别是非对映选择性往往十分困难。更为挑战的是,由于亲核试剂远离金属和配体诱导的手性环境,构建1,3-非连续手性中心往往非常困难。
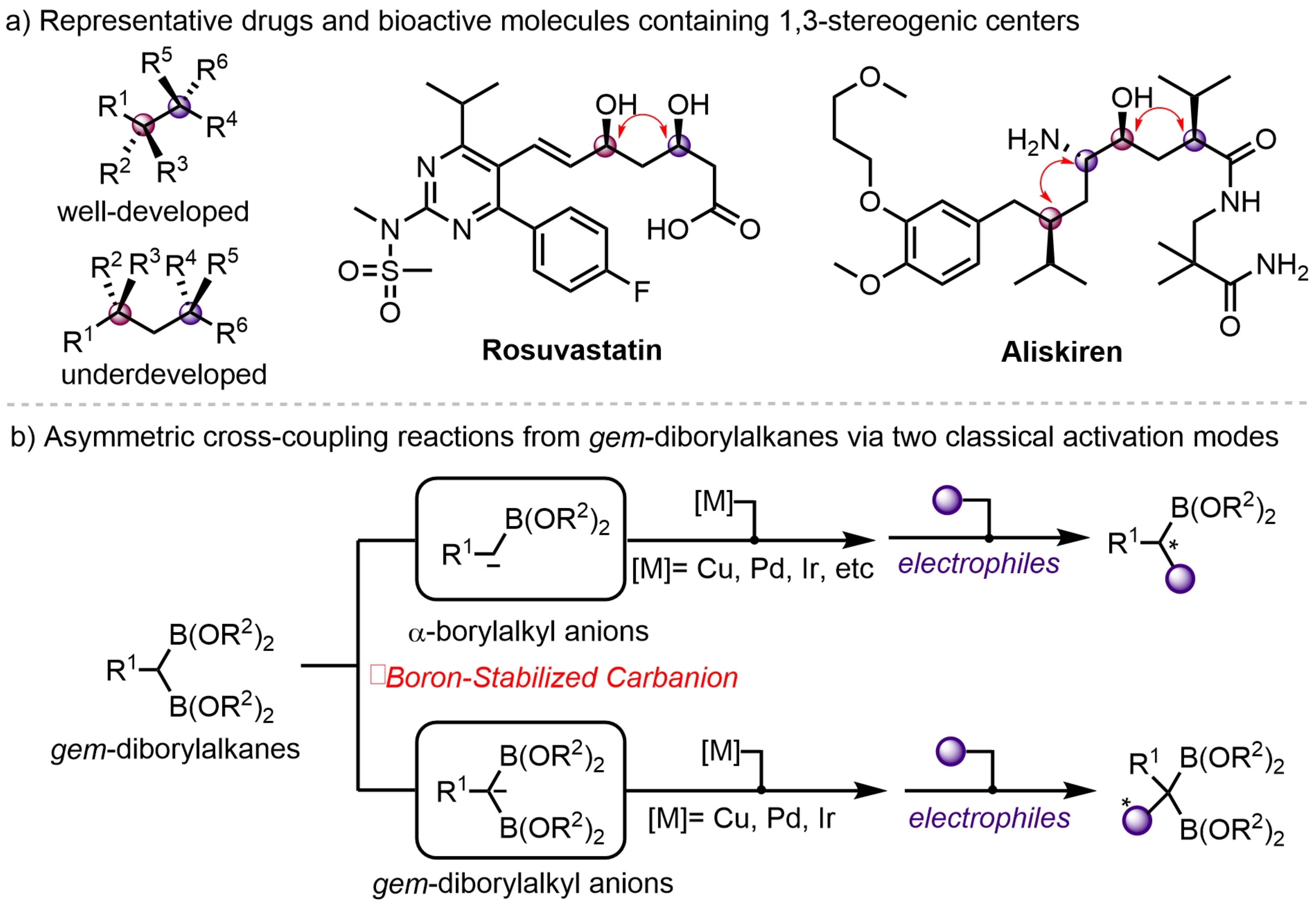
图1. 含有1,3-立体生成中心的代表性药物分子和偕二硼经典反应模式
偕二硼酸酯是合成化学中重要的转化砌块,可以通过交叉偶联、氧化、自由基反应等转化为重要的目标官能团。迄今为止,偕二硼酸酯在不对称催化反应中有两种经典的反应模式,主要通过两个关键的中间体发生反应:即α-硼烷基和偕二硼烷基阴离子(图1b)。例如:偕二硼酸酯与过渡金属发生转金属化产生α-硼烷基阴离子中间体,随后可被亲电试剂捕获,生成手性有机硼化物;在碱的协助下生成偕二硼烷基阴离子,与亲电试剂进行立体选择性转化,从而构建一系列手性有机硼酸酯。发展偕二硼酸酯新的不对称催化反应模式,将极大地拓展该类化合物在手性化学中的应用空间。
上海科技大学高得伟课题组致力于有机硼介导的新反应和新机制以及含硼药物化学的研究。本研究中,该课题组发展了一种高效合成具有高化学、区域、对映和非对映选择性的链状、非连续1,3-立体中心的1,2-双硼酸酯。值得一提的是,该工作突破了偕二硼酸酯在不对称催化反应中固有的反应模式,为构建非连续手性中心提供了新的思路。同时进一步拓展了单取代和双取代偕二硼烷在不对称反应中的化学转化空间,DFT计算阐明了高对映和非对映选择性的起源问题。此外,基于1,2-双硼酸酯中烯烃和含硼单元的多样性转化,进一步证明了该类骨架在后期官能团化转化方面的优势(图2)。
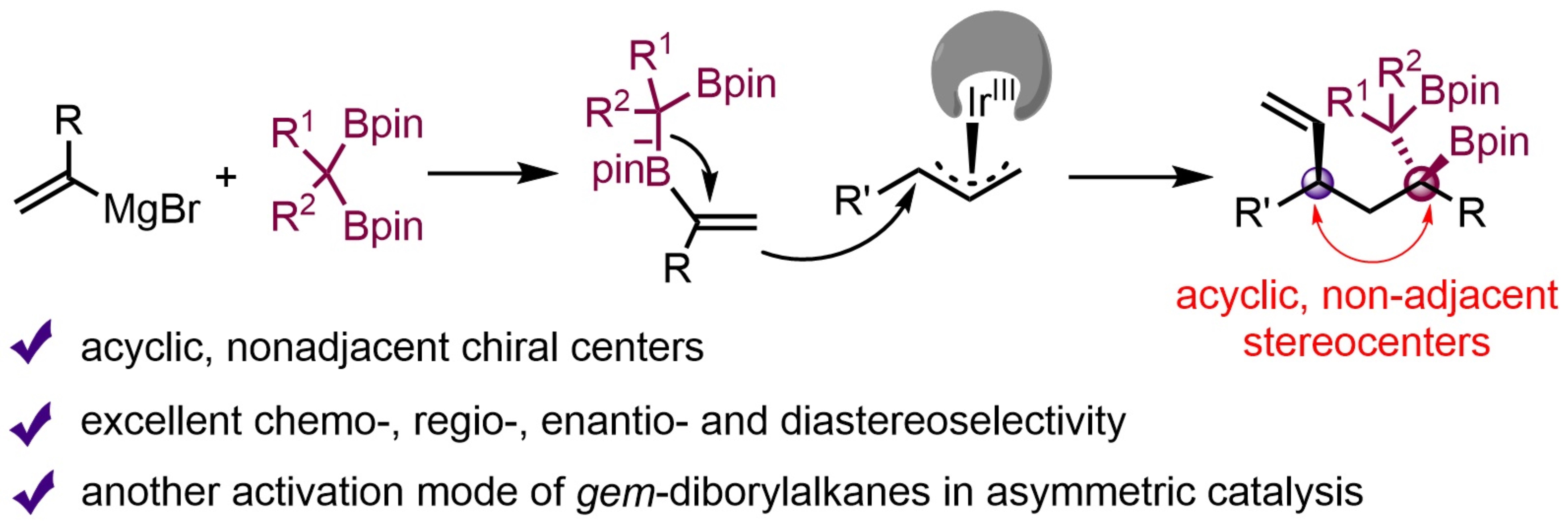
图2. 基于偕二硼催化反应模式创新构建含1,3-立体中心的1,2-双硼酸酯
高得伟课题组博士研究生蒋夏敏为论文的第一作者,高得伟教授为通讯作者,上海科技大学为唯一通讯单位。
论文标题:Asymmetric Synthesis of Chiral 1,2-Bis(Boronic) Esters Featuring Acyclic, Non-Adjacent 1,3-Stereocenters
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202318441


 沪公网安备 31011502006855号
沪公网安备 31011502006855号