10月2日, Journal of the American Chemical Society 期刊在线发表了上海科技大学iHuman研究所刘志杰及华甜课题组与中国科学院生物物理研究所王江云课题组的合作研究论文,题为:A Genetically Encoded F-19 NMR Probe Reveals the Allosteric Modulation Mechanism of Cannabinoid Receptor 1。该研究首次通过基因密码子扩展方法,在昆虫细胞表达系统中实现含氟非天然氨基酸(3-三氟甲基-L-苯丙氨酸,mtfF)的插入,并成功用于大麻素受体CB1 (cannabinoid receptor 1) 别构调节机制的研究。
氟原子由于具有对蛋白质环境变化的高度敏感性,100 %天然丰度及没有背景信号等特点,被广泛用于蛋白质动态构象的研究。目前主要通过蛋白质的半胱氨酸标记含氟原子基团,进而实现19F-NMR信号的检测。但该方法存在很多局限性,例如:需要在目标蛋白表面的感兴趣位点附近存在半胱氨酸残基(Cys),否则需要通过定点突变引入Cys;近2/3的人源G蛋白偶联受体(GPCR)含有超过10个Cys,这些多余的Cys将影响19F-NMR信号检测的精确度,因此需要将非兴趣点的Cys突变掉,但这往往会影响蛋白质的结构稳定性甚至功能;隐藏在蛋白质疏水核心内的残基不可能通过这种方法进行19F标记。鉴于Cys标记方法的局限性,王江云课题组发展了简单便捷的真核系统蛋白质氟探针标记方法并可以对GPCR进行精准的定点标记。
大麻素受体CB1是人大脑里表达量最高的GPCR之一,调控多种重要的生理活动,是治疗神经和精神类疾病、肥胖、疼痛等疾病的重要靶点。刘志杰/华甜课题组一直聚焦于大麻素受体结构与功能的系统研究,在过去几年中成功解析了大麻素受体CB1和CB2在拮抗状态、类激活和激活状态下的三维结构,揭示了正构调节配体对大麻素受体的作用机制。为了进一步探究别构调节剂对CB1的调控机理以及不同配体如何对GPCR的动态构象进行调控等重要科学问题,刘志杰/华甜课题组与王江云课题组以及iHuman研究所核磁共振实验室副研究员刘东升合作,利用基因密码子扩展方法,首次获得真核细胞内识别含氟非天然氨基酸的mtfF-氨酰-tRNA合成酶,在昆虫细胞中实现CB1构象变化敏感位点的标记。借助上海科技大学iHuman研究所核磁共振平台,研究了不同正构配体以及别构调节剂Org27569对CB1的动态构象变化的调控(图1),首次发现了Org27569 和激动剂如何在 CB1 激活过程中协同稳定以前未被识别的预激活状态。
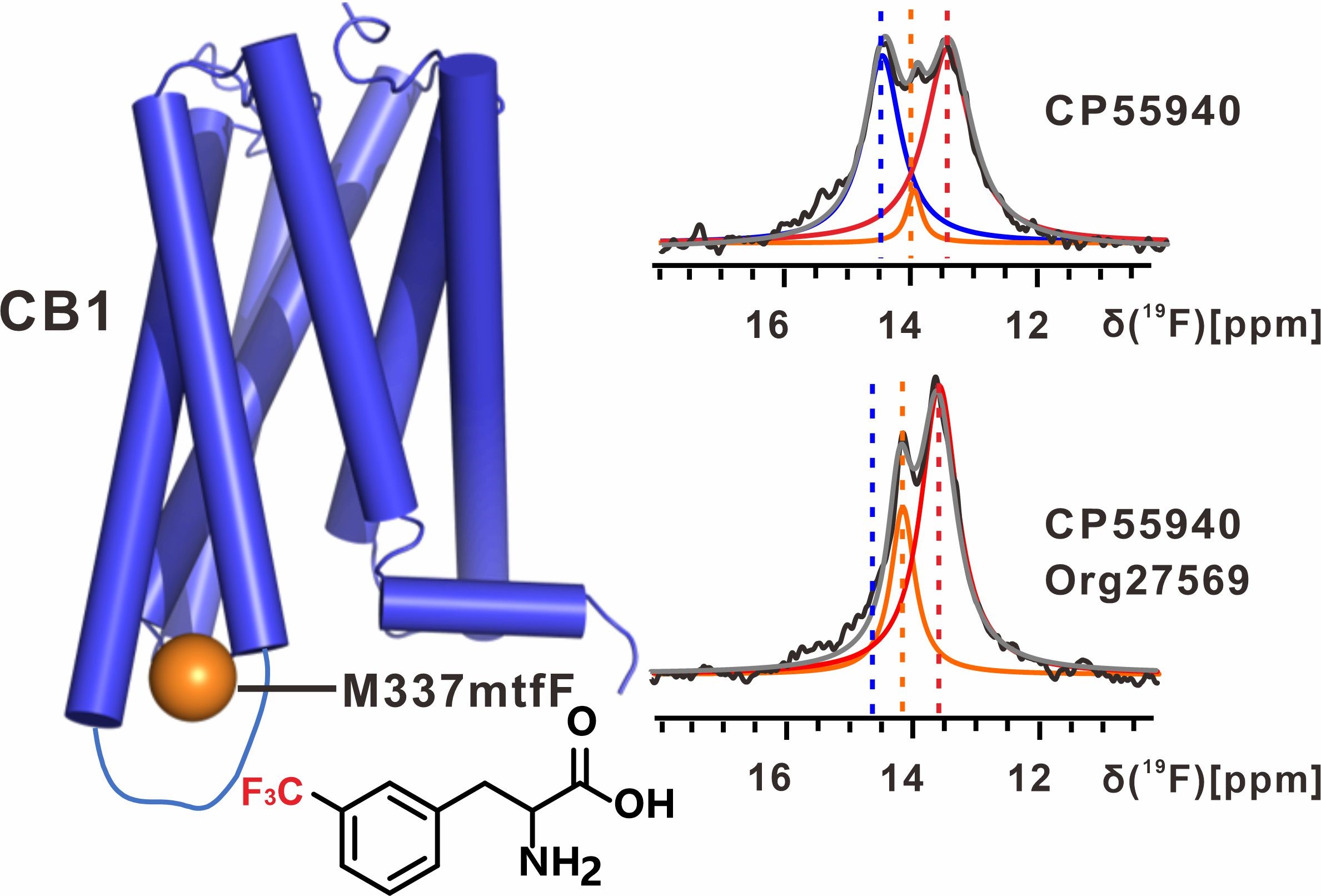
图1. 基因编码3-三氟甲基-L-苯丙氨酸研究CB1的动态构象
通过团队的密切合作和不懈努力,使用 19F-NMR 破译了受体的动态过程和多态性,同时结合X-射线晶体学方法,揭示了别构调节剂Org27569对CB1的独特调控机理,提出了CB1的激活和别构调节模型,尤其是Org27569和胆固醇分子在CB1激活过程中扮演的不同角色(图2)。该团队基于基因编码的非天然氨基酸mtfF建立了可广泛用于GPCR动态构象变化研究的标记系统,这个方法也可以用于其它真核蛋白质动态构象的研究。
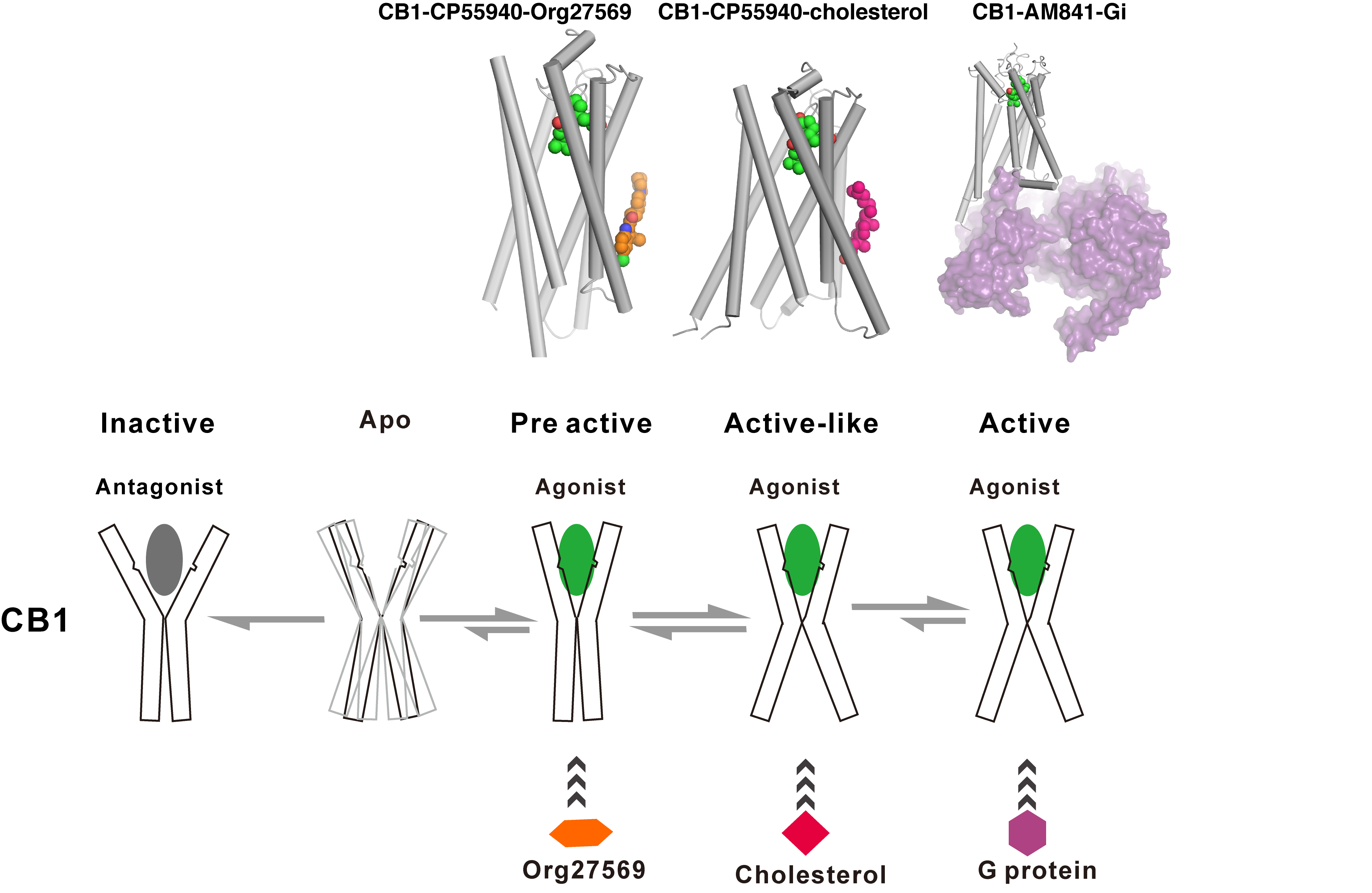
图2. CB1的激活和别构调节机制
该研究由上海科技大学iHuman研究所和中国科学院生物物理研究所共同完成。生物物理研究所核酸生物学重点实验室研究员、上海科技大学特聘教授王江云,上海科技大学刘志杰和华甜为本文的共同通讯作者,生物物理研究所王晓燕,iHuman研究所刘东升,生命学院2018级博士研究生沈灵及生物物理研究所副研究员李发慧为本文共同第一作者,上海科技大学为第一完成单位。该研究得到国家自然科学基金委和国家高技术研究发展计划资助项目的经费支持。


 沪公网安备 31011502006855号
沪公网安备 31011502006855号