大脑的神经元从出生后几乎就没有再生能力,因此临床上对于因神经元缺失和连接受损导致的相关疾病如脑卒中、帕金森综合征和阿尔治海默症等缺少有效治疗措施。神经干细胞的脑移植,替换丢失神经元或重构受损神经连接是潜在的治疗方式之一。
近日,我校生命学院何水金课题组与南京医科大学刘妍课题组合作,首次报道了移植的微型人源大脑类器官(small human cerebral organoids)在小鼠的前额叶皮质内侧区(medial prefrontal cortex, mPFC),不仅可与宿主大脑建立远距离的长投射连接,并增强了小鼠的恐惧记忆能力。该研究扩展了微型类脑器官的潜在治疗价值,也为理解类器官参与宿主大脑建立神经网络连接提供新的依据。
该研究以Human cerebral organoids establish subcortical projections in the mouse brain after transplantation(人脑类器官移植后在小鼠大脑建立皮质下投射)为题,在线发表于知名学术期刊Molecular Psychiatry(《分子精神病学》)。
神经干细胞治疗的难点是受损神经环路重构的有效性和特异性。研究团队成员前期摸索建立了高效的人源类器官分化技术,并在此基础上进一步改进了人源干细胞分化大脑谷氨酸能神经元的微型类器官的方法。研究人员将分化得到的谷氨酸能神经类器官移植到免疫缺陷小鼠(severe combined immunodeficient mice)的mPFC区, 发现绿色荧光蛋白标记的人神经纤维可进行远端投射,延伸至下丘脑外侧区(lateral hypothalamus,LH)。
团队成员进一步通过逆行示踪技术,发现下丘脑外侧区接收了移植的人类脑器官谷氨酸能神经元与内源性mPFC区神经元相似的神经支配。功能性研究表明,移植的人谷氨酸能神经元表现出成熟神经元的电生理特性,接受自身和宿主的神经递质调控。他们进一步对带有光敏感蛋白ChR2(channelrhodopsin-2)的人源谷氨酸能神经元进行光遗传操控,通过电生理手段证实移植的人源类脑器官谷氨酸能神经元可以与小鼠宿主神经元建立双向联系,并整合到宿主神经网络系统。行为学检测表明移植的微型类器官增强了小鼠的恐惧记忆环路。
该论文中,何水金课题组2015级博士研究生陈鑫和南京医科大学硕士研究生董新和博士研究生徐仕博为共同第一作者,何水金教授和刘妍教授为本文的共同通讯作者。该研究得到了科技部、上海市科委及上科大科研启动基金的支持。
论文链接:https://www.nature.com/articles/s41380-020-00910-4
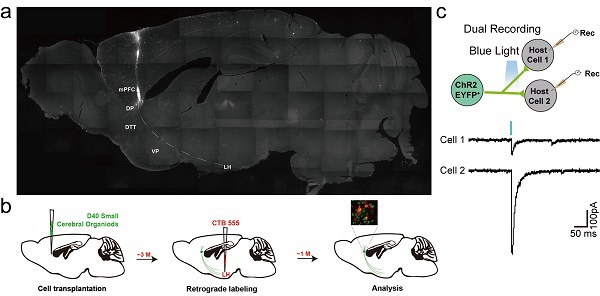
图:a,GFP荧光标记的人谷氨酸能神经元可实现多脑区远端投射;b, LH区逆行性示踪人谷氨酸能神经元投射;c,光刺激诱导小鼠宿主神经元产生突触后电流(postsynaptic currents, PSCs)。


 沪公网安备 31011502006855号
沪公网安备 31011502006855号