近日,上海科技大学iHuman研究所Wolfgang Baumeister课题组、Raymond Stevens课题组联合德国马克斯·普朗克生物化学研究所研究团队,在《美国国家科学院院刊》(PNAS)上发表题为“Cryo-EM structure of locked spike glycoprotein from bat SARS-like coronavirus WIV1, molecular dynamics and biophysics across host range”的研究成果,解析了蝙蝠来源SARS样冠状病毒WIV1刺突糖蛋白在“锁定”状态下的高分辨率冷冻电镜结构,系统揭示了其通过亚油酸分子调控实现跨物种受体识别的分子机制。

WIV1是一种从中国云南中菊头蝠中分离的类SARS冠状病毒,能够利用多种哺乳动物的ACE2作为受体,被认为具有潜在的跨种传播风险。其刺突蛋白是介导病毒进入宿主细胞的关键分子机器,也是中和抗体和疫苗设计的核心靶点。WIV1的结构信息极为有限,尤其缺乏其在“锁定”状态下的高分辨率结构。
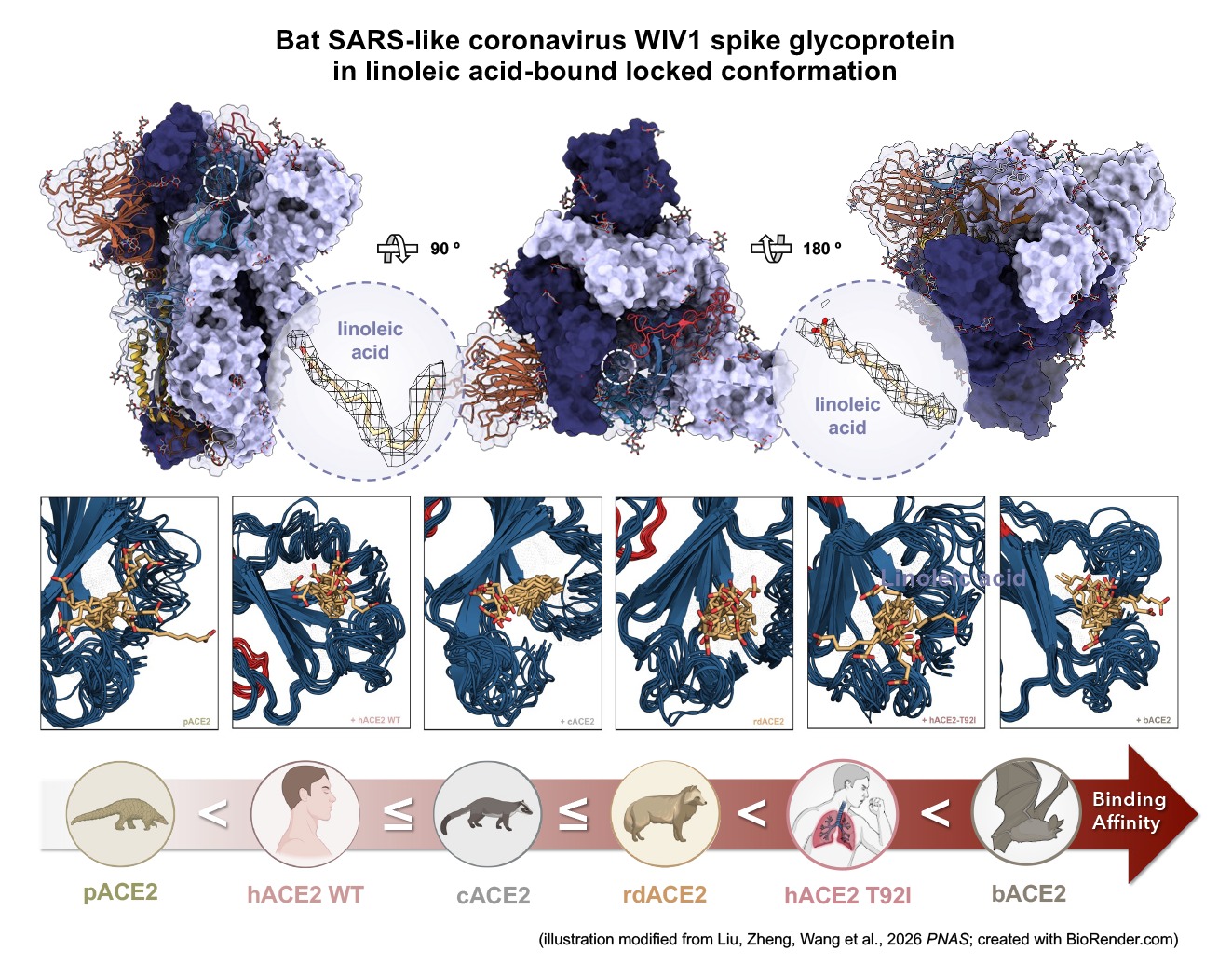
本研究通过冷冻电镜技术解析了WIV1刺突蛋白在融合前状态的高分辨率结构,发现其三聚体的每个RBD结构域均结合一个亚油酸分子,形成类似SARS-CoV-1和SARS-CoV-2中“锁定-1”构象的紧密结构。该构象通过亚油酸与RBD之间的多重疏水作用和氢键网络维持,使RBD保持在“向下”位置,避免过早暴露于免疫系统。
结合分子动力学模拟,系统分析WIV1的RBD与蝙蝠、果子狸、貉、穿山甲及人ACE2形成复合物后亚油酸的动态行为。结果显示,在所有体系中,亚油酸均未脱离其结合口袋,但其极性头部在不同宿主ACE2作用下发生不同程度的位移,导致“解锁”过程差异显著。尤其是在与人ACE2结合时,亚油酸的重定位最为显著,提示WIV1可能已具备一定的人源感染分子基础。
为进一步验证上述发现,研究人员通过质量光度法和微量热泳动实验,对WIV1 RBD与不同宿主ACE2的结合亲和力进行了定量测定。结果显示,其对蝙蝠和人ACE2(尤其是T92I突变型)具有最高亲和力,而对果子狸、貉和穿山甲ACE2的结合较弱。这一“亲和力梯度”与分子动力学模拟结果高度一致,表明WIV1在保持对天然宿主适应性的同时,也具备跨越物种屏障的潜在能力。
该工作首次系统揭示了WIV1刺突蛋白在“锁定”状态下的三维结构及其在跨宿主识别中的动态调控机制,填补了此类病毒结构生物学研究的重要空白。相关成果不仅为深入理解冠状病毒的宿主适应性与跨种传播机制提供了关键结构基础,也为广谱抗冠状病毒药物和疫苗的理性设计提供了重要理论依据,同时为相关病毒的风险评估与监测提供了分子层面的参考。
德国马普生化所博士研究生/上海科技大学iHuman研究所访问学生刘川、上海科技大学生命科学与技术学院2023级博士研究生郑晶晶和2025级博士研究生王宇涵为该论文的共同第一作者;上海科技大学iHuman研究所副研究员Luca Zinzula、孙立萍、张晓骁以及Wolfgang Baumeister教授为该论文的共同通讯作者。上海科技大学为第一完成单位。


 沪公网安备 31011502006855号
沪公网安备 31011502006855号